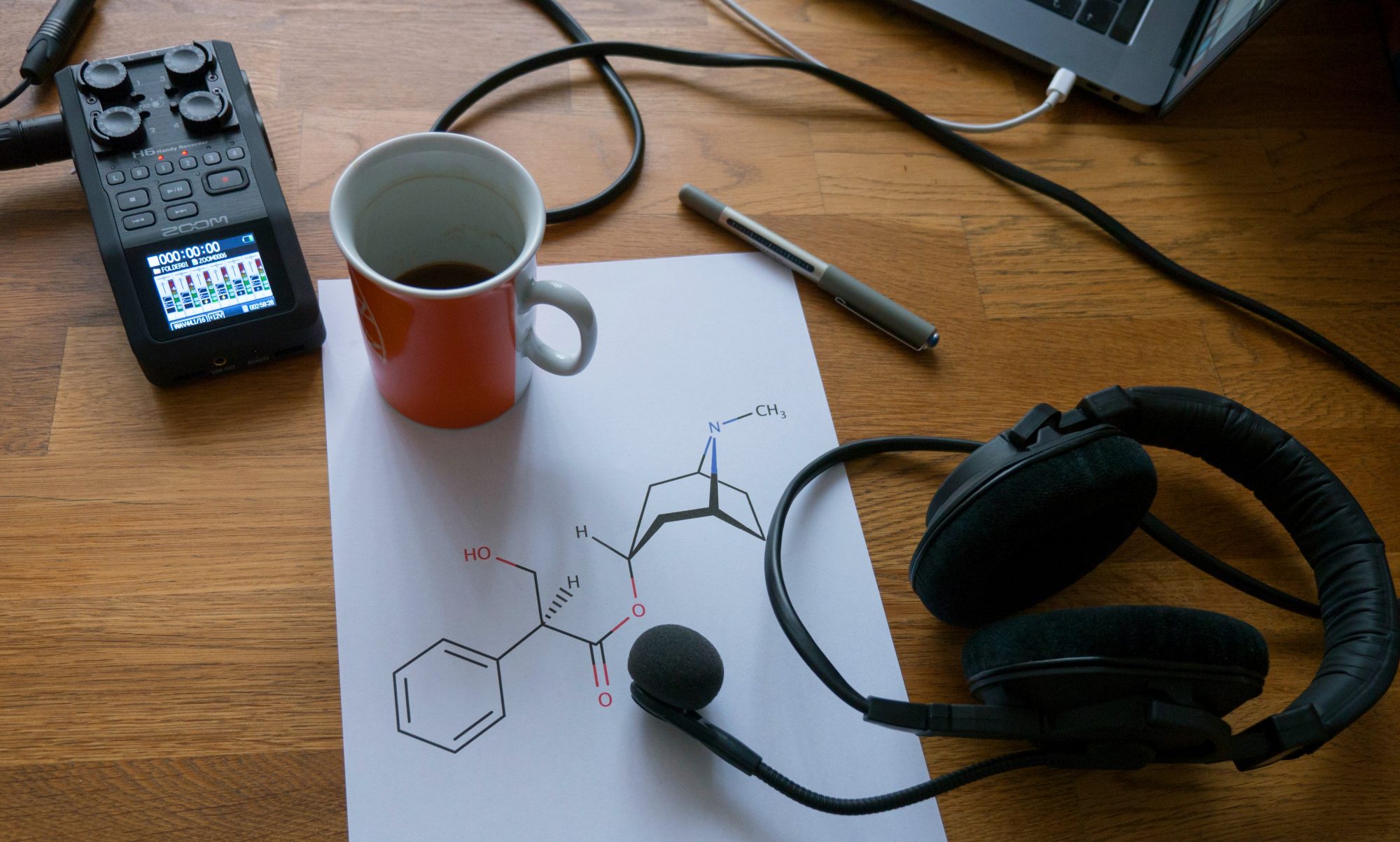
In dieser Episode sprechen Hans-Dieter Höltje und Bernd Rupp über eine weitere Klasse von Nukleohormonen, nämlich die Sexualhormone. Diese Hormone lassen sich in drei Gruppen unterteilen: Estrogene, Gestagene und Androgene.

(Im Podcast gibt es Kapitelmarken, die den Zwischenüberschriften hier im Text entsprechen, so dass es einfacher ist, bestimmte Teile erneut zu hören. Nicht jede Kapitelmarke hat eine Zwischenüberschrift, manchmal fassen wir mehrere Kapitel zusammen.)
Neuigkeiten und Feedback

Wir haben neue Sticker für das Wirkstoffradio, wenn Ihr auch welche abhaben wollt. Dann schreibt uns unter info@wirkstoffradio.de eine Mail mit eurer Adresse.
Noch mehr Merch, auch mit dem neuen Design gibt es in unserem Fanshop unter: https://wirkstoffradio.de/shop.
Einführung in die Steroidhormone
-
- Steroidhormon – Wikipedia Artikel
- Sexualhormone oder Geschlechtshormone – Wikipedia Artikel
- Nebenniere – Wikipedia Artikel
- Corticoide oder Nebennierenrindenhormone – Wikipedia Artikel
Was ist ein Steroid
-
- Steroide – Wikipedia Artikel

Die räumliche Struktur des Cyclohexan
-
- Cyclohexan – Wikipedia Artikel

Cholesterol
-
- Cholesterol – Wikipedia Artikel

Biosynthese des Progesteron
-
- Progesteron – Wikipedia Artikel
- Adolf Butenandt – Wikipedia Artikel

Biosynthese des Testosteron
-
- Testosteron – Wikipedia Artikel
- Ernst Laqueur – Wikipedia Artikel

Biosynthese des Estrogen

Funktion der Estrogene
-
- Geschlechtsmerkmal – Wikipedia Artikel
- Eierstock – Wikipedia Artikel
- Plazenta – Wikipedia Artikel
- extragenital – DWDS – Digitales Wörterbuch der deutschen Sprache
- Lipidanabolismus – Wikipedia Artikel
- Stoffwechsel – DocCheck Flexikon
- Subkutan – Wikipedia Artikel
Anwendung der Estrogene
-
- Substitution – Wikipedia Artikel
- Prostatakarzinom – Wikipedia Artikel
- Kontrazeption – DocCheck Flexikon
First Pass Effekt bei den Sexualhormonen
-
- Oral – Wikipedia Artikel
- First-Pass-Effekt – Wikipedia Artikel
Biotransformation zum Estron
-
- Estron – Wikipedia Artikel
- Wasserstoffbrückenbindung – Wikipedia Artikel

Weitere Oxidation zum Estriol
-
- Estriol – Wikipedia Artikel
- Cytochrome – Wikipedia Artikel
- Häm – Wikipedia Artikel

Oral verfügbares Ethinylestradiol
-
- Ethinylestradiol – Wikipedia Artikel

oral verfügbare Ester des Estradiol
-
- Estradiolbenzoat – Wikipedia Artikel
- Intramuskuläre Injektion – Wikipedia Artikel
Nichtsteroidale Estrogene
-
- Diethylstilbestrol – Wikipedia Artikel

Pflanzenoestrogen
-
- Isoflavonoide – Wikipedia Artikel
- Sojabohne – Wikipedia Artikel
- Genistein – Wikipedia Artikel

Raloxifen als Antiestrogen
-
- Antiestrogen – Wikipedia Artikel
- Raloxifen – Wikipedia Artikel
- Thiophen – Wikipedia Artikel
- Piperidin – Wikipedia Artikel
- Tertiär (Chemie) – Wikipedia Artikel

Raloxifen Bindung
-
- Estrogenrezeptor – Wikipedia Artikel
- Kompetitive Hemmung – Wikipedia Artikel
- Brustkrebs – Wikipedia Artikel
- Mammakarzinom – DocCheck Flexikon
- Kristallstruktur des RaloxifenKomplex: 7KBS

Biosynthese Blocker
-
- Aromatasehemmer – DocCheck Flexikon
- Aromatase inhibitor – Wikipedia Artikel (englisch)
- Cytochrome P450 19A1 – Wikipedia Artikel (englisch)
- Cytochrome P450 19A1 – DrugBank Online
- Triazole – Wikipedia Artikel
- IsoPropylgruppe – Wikipedia Artikel
- Nitrilgruppe – Wikipedia Artikel
- Anastrozol – Wikipedia Artikel

Nichtkompetitive Hemmstoffe
-
- Nichtkompetitiver Antagonist – Wikipedia Artikel
- Enzymhemmung – Wikipedia Artikel
- irreversible Bindung – Wikipedia Artikel
- Kovalente Bindung – Wikipedia Artikel
- Funktionelle Gruppe – Wikipedia Artikel
Exemestan
-
- Exemestan – Wikipedia Artikel
- Vinylgruppe – Wikipedia Artikel

Exkurs: Herkunft der Bezeichnung Estrogen
Gestagene
-
- Gestagene – Wikipedia Artikel
- Gestation = Schwangerschaft – Wiktionary
- Gelbkörper oder Corpus luteum – Wikipedia Artikel
Biotransformation der Gestagene
-
- Glutaminsäure – Wikipedia Artikel
- Glutamin – Wikipedia Artikel
- Carboxamidgruppe – Wikipedia Artikel
- Reduktion (Chemie) – Wikipedia Artikel
Verlängert wirkende Gestagene
-
- Steroid-17alpha-Hydroxylase – Wikipedia Artikel

Oral verfügbares Gestagen Chlormadinonacetat
-
- Chlormadinon – Wikipedia Artikel

Die Inhoffen Geschichte: Ethinyltestosteron ein Gestagen
-
- Schering AG – Wikipedia Artikel
- Hans Herloff Inhoffen – Wikipedia Artikel
- Kontrazeptiva – Wikipedia Artikel
- Ethisterone – Wikipedia Artikel (englisch)
- Norethisteron – Wikipedia Artikel
- Blockbuster – Wikipedia Artikel

Kristallstruktur mit Norethisteron
-
- Kristallstruktur von Norethisteron im Progesteron Rezeptor PDB-ID: 1SQN

Antigestagene
-
- Mifepriston – Wikipedia Artikel
- Schwangerschaftsabbruch – Wikipedia Artikel

Androgene
Testosteron
-
- Testosteron – Wikipedia Artikel

Wirkform von Testosteron
-
- Dihydrotestosteron – Wikipedia Artikel
- Prohormon – Wikipedia Artikel

Wirkung des 5-alpha-Dihydrotestosteron
-
- Steroid-5alpha-Reduktase – Wikipedia Artikel
- Proteinanabole Wirkung – Wikipedia Artikel
- Doping – Wikipedia Artikel
- Virilisierung = Vermännlichung – Wikipedia Artikel
- Mammakarzinom – DocCheck Flexikon
oral verfügbares Androgen Mesterolon
-
- Mesterolone – Wikipedia Artikel (englisch)
- Mesterolon – DocCheck Flexikon

Oral verfügbare Ester
-
- Intramuskuläre_Injektion – Wikipedia Artikel
- Testosterone_propionate – Wikipedia Artikel (englisch)
Transport der Steroide im Körper
-
- Transportprotein – Wikipedia Artikel
Biotransformation der Androgene
-
- Androsteron – Wikipedia Artikel

Nandrolon als Beispiel Anabolikum
-
- Nandrolon – Wikipedia Artikel
- Decansäure – Wikipedia Artikel
- Magersucht – Wikipedia Artikel
- Tiermast – Wikipedia Artikel

Antiandrogen Cyproteron-acetat
-
- Cyproteron – Wikipedia Artikel
- Cyclopropan – Wikipedia Artikel

Flutamid
-
- Flutamid – Wikipedia Artikel
- Hydroxyflutamide – Wikipedia Artikel

Finasterid als 5alpha-Reduktase-Hemmer
-
- Finasterid – Wikipedia Artikel
- 5-Alpha-Reduktasehemmer – DocCheck Flexikon
- Benigne Prostatahyperplasie – DocCheck Flexikon
- Benigne = Gutartig – Wiktionary
- Maligne = Bösartig – Wiktionary
- Malignität – Wikipedia Artikel

Abschluss der Steroide
Jahresrückblick 2023
Bernd bedankt sich bei allen Interview Partnern diese Jahres und natürlich auch bei Hans-Dieter, ohne deren Mithilfe das Wirkstoffradio nicht möglich wäre. Vielen Dank an:
-
- Prof. Dr. Daniel Lauster – Fachbereich Biologie, Chemie, Pharmazie
- WSR062 MUCPEP: Wirkstoffmodelle für die Mukoviszidose Therapie – Interview mit Dr. Daniel Lauster
- Dr. Christine Rohde – Leibniz Institut DSMZ
- WSR065 Phagen: Auf der Jagd nach Bakterienfressern – Interview mit Dr. Christine Rohde
- Prof. Dr. Yvonne Mast – Leibniz Institute DSMZ
- WSR066 Die unentdeckte Vielfalt der Aktinomyceten: Neue Wege zur Synthese von Wirkstoffen – Interview mit Prof. Dr. Yvonne Mast
- Prof. Dr. Lea Ann Dailey – Universität Wien
- WSR068 Pharmazeutische Technologie und Biopharmazie: Nanopartikel in Arzneiformen – Interview mit Prof. Dr. Lea Ann Dailey
- Dr. Norbert Arnold – Leibniz-Institut für Pflanzenbiochemie (IPB)
- WSR070 Pilze: Von Goldschimmel, Hautköpfen und Scheinbuchen – Interview mit Dr. Norbert Arnold
- 37C3 – CCC Event Blog
- Wissen(schaft)spodcasts.de – Homepage
Liebe Hörer:innen, Ihr wollt uns eine AUA-Frage stellen, dann schreibt uns unter dem Betreff [AUA-Frage] an info@wirkstoffradio.de. Oder auf X (Twitter) an @wirkstoffradio mit dem Hashtag #AUAFrage, das geht dort auch als Direktnachricht.
Wir freuen uns immer über Feedback: per Mail unter info@wirkstoffradio.de, in den Kommentaren unter den einzelnen Episoden, über X (Twitter) @wirkstoffradio, bei Matodon unter @wirkstoffradio@podcasts.social oder auch als Bewertung bei iTunes/Apple-Podcasts oder panoptikum.social.
Wirkstoffradio-Feedback-Telefon +49 (0)30 746 910 64
In unserem Fanshop können sich Hörer:Innen mit Wirkstoffradio Merch wie T-Shirts, Hoodies, Basecaps aber auch Tassen und Einkaufsbeutel ausstatten.
Wirkstoffradio ist lizenziert unter einer Creative Commons Namensnennung - Keine Bearbeitungen 4.0 International Lizenz.